 Лейкоз (син. – лейкемия) – это онкологическое заболевание, возникающее в костном мозге вследствие мутаций стволовых клеток. Результатом подобных мутаций является потеря способности клеток крови развиваться до зрелых форм. Как любое злокачественное заболевание лейкозы имеют морфологический субстрат – бластные клетки. Неконтролируемый рост бластных клеток, их неспособность полноценно выполнять свои функции и вытеснение центров нормального кроветворения, обуславливают симптомы заболевания.
Лейкоз (син. – лейкемия) – это онкологическое заболевание, возникающее в костном мозге вследствие мутаций стволовых клеток. Результатом подобных мутаций является потеря способности клеток крови развиваться до зрелых форм. Как любое злокачественное заболевание лейкозы имеют морфологический субстрат – бластные клетки. Неконтролируемый рост бластных клеток, их неспособность полноценно выполнять свои функции и вытеснение центров нормального кроветворения, обуславливают симптомы заболевания.
Выделяют острые лейкозы и хронические. Важно отметить, что острый лейкоз не может перейти в хронический, а хронический обостриться. Терминами острый и хронический обозначают не характер течения процесса, а абсолютно разные болезни. В зависимости от того, какие клетки костного мозга поражены, лейкозы подразделяют на лимфобластные и миелоидные формы. В свою очередь лимфоидный лейкоз может быть Т и В клеточным. В первом случае бластные клетки являются незрелыми предшественниками Т лимфоцитов, во втором – В лимфоцитов. Острый миелоидный лейкоз может быть нескольких видов: из предшественников эритроцитов, тромбоцитов, нейтрофилов и пр. В отличие от острого миелоидного лейкоза, при хронической форме, превалируют более зрелые клетки крови. Самым распространенным и благоприятным является острый лимфобластный лейкоз. Хронический лимфобластный лейкоз у детей не встречается.
Среди детских онкологических болезней лейкозы занимают первое место, что составляет около 35%. Наиболее часто болеют дети в возрасте от 2 до 5 лет. Риск развития лейкоза по статистике незначительно выше у мальчиков.
Причины лейкозов у детей.
На сегодняшний день ученым еще не удалось окончательно установить причину возникновения лейкозов у детей, однако разработан ряд убедительных теорий, подтверждаемых современными научными исследованиями. Одной из наиболее распространенных теорий является генетическая. Согласно ей, в результате случайных изменений хромосом, возникающих внутриутробно у плода, формируются аномальные гены. Они запускают производство аномальных веществ, блокирующих нормальное созревание клеток крови.
Второй, не менее распространенной теорией является вирусная. Очень часто в практической деятельности врач сталкивается с ситуацией, когда лейкоз у ребенка развивается на фоне недавно перенесенной вирусной инфекции. Как правило, это инфекционный мононуклеоз, ветряная оспа, аденовирусная инфекция. Вероятнее всего вирусы приводят к возникновению лейкоза путем встраивания в клеточный геном и вызывая в нем различные поломки. Помимо этого, вирусная инфекция приводит к чрезмерно активному делению иммунных клеток, что так же можно отнести к фактору риска. Во многих лейкозных клетках можно обнаружить геном того или иного вируса, что является убедительным подтверждением данной теории.
Теория иммунодефицита. Всем известно, что иммунная система человека выполняет одну из важнейших функций – уничтожение чужеродных микроорганизмов и веществ, попавших к нам в организм. Однако помимо борьбы с агентами, попавшими извне, иммунная система направлена на уничтожение наших собственных патологически измененных клеток, в том числе и злокачественных. При снижении иммунитета эта функция не осуществляется в полном объеме, что создает благоприятную почву для неконтролируемого роста бластных клеток.
Вторичное развитие лейкозов. Современные схемы лучевой и химиотерапии позволили добиться значительных успехов в излечении детей от онкологических заболеваний. Но на обратной стороне медали скрываются отдаленные последствия подобного лечения. Речь идет о развитии вторичных опухолей, в том числе и лейкозов.
Облучение матери во время беременности (рентген, компьютерная томографя), употребление алкоголя, наркотических веществ и курение, так же является фактором риска в развитии лейкозов у детей. Также повышен риск развития лейкозов у детей уже с имеющимися генетическими заболеваниями, такими как синдром Дауна.
Симптомы лейкоза.
В течении лейкоза выделяют несколько стадий. Каждая имеет свои особенности.
1. Предлейкозный период. Этот период характеризуется отсутствием ярких, специфических симптомов. Этот факт и является причиной поздней диагностики. Основными признаками болезни, которые могут отметить родители в предлейкозном периоде, являются: слабость, утомляемость ребенка в школе или детском саду. Сниженный аппетит, пониженное настроение. Ребенок предпочитает сон и отдых подвижным играм. Так же возможны разнообразные нарушения стула, от запоров до диарейного синдрома. Часто удается зафиксировать повышение температуры тела до 37-37,5 С. Как правило, такие неспецифические симптомы трактуются родителями и врачами, как начало ОРВИ.
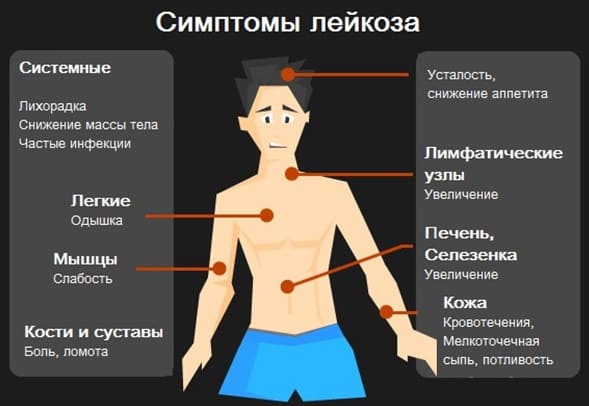
2. Острый период отличается яркими симптомами. Температура тела может повышаться до 38 градусов и выше. Ребенок теряет вес даже при калорийном питании. Общее самочувствие ухудшается. Одним из характерных симптомов при лейкозах является анемия (малокровие), которая проявляется бледностью кожи. Из-за снижения количества тромбоцитов в крови часто развивается кровоточивость. Как правило, это мелкоточечная сыпь на коже и слизистой оболочек полости рта. Возможны носовые кровотечения, а так же более грозные симптомы, такие как почечные и желудочно-кишечные кровотечения. Ребенок может жаловаться на боли в костях и суставах, потливость по ночам, кожный зуд. Очень часто увеличиваются лимфатические узлы в области шеи, над ключицами, в паху. В отличии от воспалительного увеличения лимфатических узлов, при лейкозах они безболезненные, кожа над ними не изменена. Больше чем у половины маленьких пациентов увеличивается в размерах печень и селезенка. Достоверно определить это может только врач, но в случае значительного увеличения этих органов у ребенка будет увеличен и деформирован живот, что сразу отметят внимательные родители.
3. После начала лечения острый период сменяет фаза ремиссии. Состояние ребенка стабилизируется, печень, селезенка и лимфатические узлы уменьшаются в размерах. Костный мозг начинает вырабатывать достаточное количество полноценных клеток, что обуславливает нормальное самочувствие ребенка.
4. После завершения всего курса лечения, как правило, ребенка можно считать полностью здоровым, но в ряде случаев возможен рецидив. Данная фаза проявляется схожими симптомами с острым периодом.
Болезни, с которыми можно спутать лейкоз.
На ранних этапах болезни представляет большую трудность отличить лейкоз от вирусных инфекций, таких как инфекционный мононуклеоз, аденовирусная инфекция и банальная ОРВИ. Все они могут протекать с увеличением лимфатических узлов, слабостью, повышением температуры тела. Бледность кожи, может возникать при анемиях другой природы: железодефицитная, В12 дефицитная, апластическая. Кровоточивость часто бывает при таких заболеваниях, как гемофилия, тромбоцитопеническая пурпура. Болевой синдром в костях и суставах может развиваться при ревматологических болезнях – ювенильный ревматоидный артрит, системная красная волчанка. Учитывая тот факт, что лейкозы могут маскироваться под разнообразные заболевания, необходимо сразу обращаться за медицинской помощью и не заниматься самолечением.
При наличии подобных жалоб у ребенка, необходимо обратится к участковому педиатру. Врач в свою очередь определит, есть ли необходимость консультации более узкого специалиста – детского онколога/гематолога.
Диагностика лейкоза.

В случае, когда есть подозрение на лейкоз, ребенка обязательно госпитализируют в онкогематологический стационар. Пребывание дома при подобном заболевании или подозрении – строго противопоказано! В течении нескольких дней специалисты возьмут все необходимые анализы и выполнят все инструментальные исследования.
Первым делом берут общий и биохимический анализ крови. В общем анализе при лейкозах часто отмечается анемия (сниженное количество эритроцитов и гемоглобина), тромбоцитопения (снижение количества тромбоцитов), количество лейкоцитов может быть как снижено, так и повышено. Иногда в крови можно обнаружить бластные клетки.
Обязательно берут костный мозг и спинно-мозговую жидкость. Анализ костного мозга является самым важным, именно на его основании устанавливают или снимают диагноз лейкоза. Спинно-мозговая жидкость является зеркалом состояния центральной нервной системы. При обнаружении в ней бластных клеток применяются более интенсивные схемы лечения.
Все остальные исследования, такие как УЗИ, компьютерная томография, рентгенография являются дополнительными и необходимы для оценки распространенности процесса.
В отличие от других злокачественных заболеваний, лейкозы не имеют стадий. В данном случае оперируют понятием группа риска. От того, в какую группу попадет ребенок, будет зависеть интенсивность лечения. Например, при остром лимфобластном лейкозе их выделяют три: стандартная, средняя и высокая группа риска. Распределение осуществляется на основании возраста пациента и исследования костного мозга. Если возраст пациента от 1 до 6 лет, количество лейкоцитов на момент постановки диагноза составляет менее 20 тысяч и отсутствуют наиболее значимые хромосомные мутации в бластных клетках, то ребенка относят и лечат по протоколу для стандартного риска. В случае обнаружения генетических мутаций, так называемой филадельфийской хромосомы, ребенок автоматически попадет в группу высокого риска и получает более интенсивную химиотерапию не зависимо от возраста и других показателей. Если возраст до 1 года или старше 6 лет и/или количество лейкоцитов составляет более 20 тысяч – пациент относится к группе среднего риска. В зависимости от группы риска врач выбирает ту или иную схему лечения. В зависимости от ответа на проводимое лечение, группа риска может изменяться, но только в худшую сторону. При хороших результатах на начальных этапах лечения, пациент все равно остается в своей первоначальной группе.
Лечение лейкоза у детй.
За последние несколько десятилетий детская онкология значительно продвинулась вперед. Если в середине прошлого столетия от лейкозов умирало более 90% пациентов, то на сегодняшний день выживаемость составляет около 80%. Другими словами 8 из 10 детей можно считать полностью излеченными при своевременных возможностях терапии.
В отличие от других областей медицины, где врач, полагаясь на свой богатый опыт, может корректировать тактику лечения и заменять один препарат на другой, в детской онкологии дело обстоит иначе. Существуют утвержденные протоколы лечения каждого злокачественного заболевания, в частности и лейкозов, от которых врач не имеет права отступать за исключением случаев непереносимости медикаментов или устойчивости опухоли.
В схеме терапии лейкозов выделяют несколько фаз: индукционная, консолидирующая, реиндуцирующая и поддерживающая. В течении всех периодов используют гормональные и противоопухолевые препараты. Часть препаратов дают в виде таблеток, но большую часть вводят внутривенно при помощи специальных устройств, инфузоматов. Данные аппараты позволяют с высокой точностью устанавливать скорость внутривенных инфузий, что является важным условием терапии лейкозов у детей.
Для пациентов из группы высокого риска, а так же у пациентов с поражением головного мозга применяют лучевую терапию.
Как правило, весь период лечения в стационаре занимает до 3-4 месяцев. Препараты поддерживающей терапии принимаются амбулаторно. При тяжелом течении заболевания, ранних рецидивах, нечувствительности опухоли к проводимому лечению, ребенок направляется на трансплантацию стволовых клеток от родственных доноров. Данный метод позволяет в большинстве случаев добиться стойкой ремиссии.
Важным компонентом является сопроводительная терапия. Она включает в себя антибактериальные, противогрибковые препараты, так как в период лечения иммунитет ребенка значительно снижен, препараты крови, такие как эритроцитная и тромбоцитная взвеси, используемые с целью замещения. Постоянная инфузия раствора глюкозы, физиологического раствора, растворов ионов калия, поддерживают ионный баланс и способствуют дезинтоксикации.
Лечение лейкозов у детей относится к высокотехнологической помощи, полис ОМС покрывает не все затраты, какую то часть покрывают благотворительные фонды. Так же возможно получить квоты на лечение в департаменте здравоохранения. Для этого необходимы документы, подтверждающие наличие заболевания (выписной эпикриз из истории болезни, результаты анализов). Данным вопросом с родителями занимается и лечащий врач.
Инвалидность. При установленном диагнозе острый лейкоз ребенок направляется на медико-социальную экспертизу. 1 группа инвалидности определяется при первично установленном диагнозе, а так же в случае обострения лейкоза. 2 группа определяется при стойкой ремиссии не менее года при продолжении специфической терапии. 3 группа определяется при полной стойкой ремиссии после окончания специфического лечения.
Прогноз.
Без лечения прогноз крайне неблагоприятный. Более чем в 90% случаев больной умирает.
При раннем распознавании и своевременно начатом лечении шанс добиться стойкой полной ремиссии достигает 80%! По статистическим данным наиболее благоприятный прогноз отмечается у детей от 1 до 6 лет с острым В-клеточным и лимфобластным лейкозом. Промежуточный прогноз при острых миелоидных лейкозах и менее благоприятный при хроническом миелоидном лейкозе. Так же неблагоприятным фактором является возраст ребенка до 1 года и старше 6 лет. Однако эта статистика достаточно условна, порой хороший ответ на лечение встречается при острых и хронических миелолейкозах.
Сказать достоверно, что влияет на прогноз и исход заболевания очень трудно. Вероятнее всего это зависит не только от вида опухоли и возраста ребенка, но и от характера изменений в геноме бластной клетки.
Врач педиатр Журавель Е.А.
Новости по теме:
Исследовательская группа из Массачусетской многопрофильной больницы совместно с Гарвардским институтом стволовых клеток выяснили, что справиться с прогрессированием острого миелоидного лейкоза поможет ингибирование одного из ферментов, участвующих в дифференцировке опухолевых клеток. Исследователям удалось обнаружить, что у 70% людей, страдающих различными формами острого миелоидного лейкоза, нарушена экспрессия транскрипционного фактора HoxA9. Ингибиторов этого белка до последнего времени обнаружено не было.
Авторы во главе с Дэвидом Сайкесом предложили новый подход к скринингу потенциальных соединений. Они изучили более трехсот тысяч веществ, что позволило им отобрать 12 веществ, предположительно обладающих необходимыми свойствами. Одиннадцать из них подавляли дифференцировку опухолевых клеток, ингибируя работу фермента DHODH. Ранее не было известно, что этот белок участвует в процессе дифференцировки миелоидных клеток.
Ученые протестировали работу ингибитора DHODHна мышах с острым миелоидным лейкозом – препарат снижал число опухолевых клеток, увеличивал продолжительность жизни животных и, что немаловажно, не вызывал побочных эффектов, характерных для большинства химиотерапевтических препаратов. Шестинедельное лечение не смогло предотвратить рецидив, а вот десятинедельный курс привел к длительной ремиссии.
После того, как будет подробно изучен механизм действия ингибитора DHODH, ученые планируют начать проводить эксперименты с участием пациентов.




