Болезнь Паркинсона, или паркинсонизм - медленно прогрессирующее состояние, которое проявляется замедленностью движений, мышечной ригидностью и тремором покоя. Заболевание впервые описано английским врачом Джеймсом Паркинсоном, который назвал его дрожательным параличом В 1877 г.
Выделяют идиопатическии паркинсонизм (болезнь Паркинсона) и синдром паркинсонизма, обусловленный различными причинами и нередко служащий проявлением иных дегенеративных заболеваний нервной системы. Болезнь Паркинсона или паркинсонизм встречается у 60—140 на 100 000 населения; его частота резко увеличивается с возрастом. Согласно статистическим данным, паркинсонизм встречается у 1 % населения до 60 лет и у 5% лиц более старшего возраста. Мужчины болеют несколько чаще, чем женщины.
Причины болезни Паркинсона
В основе болезни Паркинсона и паркинсонизма лежат уменьшение количества нейронов черной субстанции и формирование в них включений — телец Леви. Его развитию способствуют наследственная предрасположенность, пожилой и старческий возраст, воздействие экзогенных факторов. В возникновении акинетико-ригидного синдрома могут иметь значение наследственно обусловленное нарушение обмена катехоламинов в мозге или неполноценность ферментных систем, контролирующих этот обмен. Часто выявляется семейная отягощенность по этому заболеванию при аутосомно-доминантном типе наследования. Подобные случаи относят к болезни Паркинсона. Различные экзо– и эндогенные факторы (атеросклероз, инфекции, интоксикации, травмы) способствуют проявлению генуинных дефектов в механизмах обмена катехоламинов в подкорковых ядрах и возникновению заболевания.
Синдром паркинсонизма возникает в результате перенесенных острых и хронических инфекций нервной системы (клещевой и другие виды энцефалитов). Причинами болезни Паркинсона и паркинсонизма могут служить острые и хронические расстройства мозгового кровообращения, церебральный атеросклероз, сосудистые заболевания головного мозга, опухоли, травмы и опухоли нервной системы. Возможно развитие паркинсонизма вследствие лекарственных интоксикаций при длительном использовании препаратов фенотиазинового ряда (аминазин, трифтазин), метилдофы, некоторых наркотических средств – лекарственный паркинсонизм. Паркинсонизм может развиваться при острой или хронической интоксикации окисью углерода и марганца.
Основным патогенетическим звеном дрожательного паралича и синдрома паркинсонизма является нарушение обмена катехоламинов (дофамина, норадреналина) в экстрапирамидной системе. Дофамин выполняет самостоятельную медиаторную функцию в реализации двигательных актов. В норме концентрация дофамина в базальных узлах во много раз превышает его содержание в других структурах нервной системы. Ацетилхолин является медиатором возбуждения между полосатым телом, бледным шаром и черным веществом. Дофамин является его антагонистом, действуя тормозяще. При поражении черного вещества и бледного шара снижается уровень дофамина в хвостатом ядре и скорлупе, нарушается соотношение между дофамином и норадреналином, возникает расстройство функций экстрапирамидной системы. В норме импульсация модулируется в сторону подавления хвостатого ядра, скорлупы, черного вещества и стимулирования бледного шара. При выключении функции черного вещества возникает блокада импульсов, поступающих из экстрапирамидных зон коры большого мозга и полосатого тела к передним рогам спинного мозга. В то же время к клеткам передних рогов поступают патологические импульсы из бледного шара и черного вещества. В результате усиливается циркуляция импульсов в системе альфа– и гамма-мотонейронов спинного мозга с преобладанием альфа-активности, что приводит к возникновению паллидарно-нигральной ригидности мышечных волокон и тремора – основных признаков паркинсонизма.
Патоморфология болезни Паркинсона и паркинсонизма.
Основные патологоанатомические изменения при паркинсонизме наблюдаются в черном веществе и бледном шаре в виде дегенеративных изменений и гибели нервных клеток. На месте погибших клеток возникают очаги разрастания глиальных элементов или остаются пустоты.
Формы паркинсонизма:
дрожательная, дрожательно – ригидная, ригидно – дрожательная, акинетико – ригидная, смешанная.
По степени тяжести различают пять стадий болезни Паркинсона. Наибольшее распространение получила классификация, предложенная в 1967 году Хеном и Яром:
• 0 стадия — двигательные проявления отсутствуют
• I стадия — односторонние проявления заболевания
• II стадия — двусторонние симптомы без постуральных нарушений
• III стадия — умеренная постуральная неустойчивость, но пациент не нуждается в посторонней помощи
• IV стадия — значительная утрата двигательной активности, но пациент в состоянии стоять и передвигаться без поддержки
• V стадия — в отсутствие посторонней помощи пациент прикован к креслу или постели
Симптомы болезни Паркинсона и паркинсонизма
Симптомы Паркинсонизма – это нарушения движений и мышечного тонуса и их сочетания. Скованность движений, повышение тонуса, тремор рук и головы, движения нижней челюстью по типу «жевания», нарушения почерка и точности движений, походка «согнувшись», маленькими шажками, «шаркающая», бедность мимических движений – «застывшее лицо», снижение эмоциональности поведения, депрессия. Симптомы болезни, вначале односторонние, в дальнейшем прогрессируют, в тяжелых случаях приводят к инвалидизации, обездвиженности, когнитивным нарушениям.
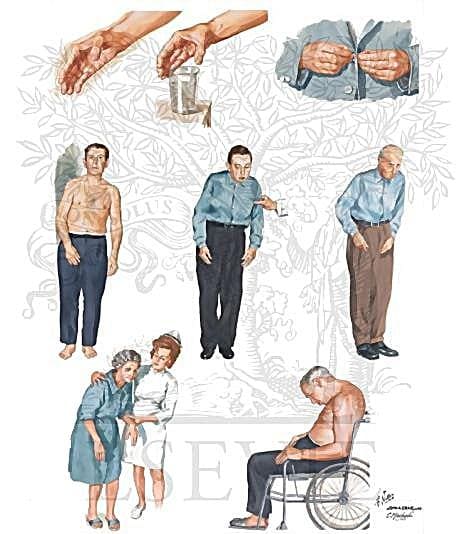
Симптомы паркинсонизма
Основной клинический синдром при болезни Паркинсона и паркинсонизма – акинетико-ригидный или гипертонически-гипокинетический. Для дрожательного паралича и паркинсонизма характерны гипо– и акинезия. Появляется своеобразная сгибательная поза: голова и туловище наклонены вперед, руки полусогнуты в локтевых, лучезапястных и фаланговых суставах, нередко плотно приведены к боковым поверхностям грудной клетки, туловища, ноги полусогнуты в коленных суставах. Отмечается бедность мимики. Темп произвольных движений с развитием заболевания постепенно замедляется, иногда довольно рано может наступить полная обездвиженность. Походка характеризуется мелкими шаркаюшими шагами. Нередко наблюдается склонность к непроизвольному бегу вперед (пропульсии). Если толкнуть больного вперед, он бежит, чтобы не упасть, как бы «догоняя свой центр тяжести». Часто толчок в грудь ведет к бегу назад (ретропульсии), в сторону (латеропульсии). Эти движения наблюдаются также при попытке сесть, встать, откинуть голову назад. Часто при резко выраженном синдроме паркинсонизма позы больного напоминают каталептические. Акинез и пластическая гипертония особенно резко проявляются в мускулатуре лица, жевательных и затылочных мышцах, мышцах конечностей. При ходьбе отсутствуют содружественные движения рук (ахейрокинез). Речь тихая, монотонная, без модуляций, с наклонностью к затуханию в конце фразы.
При пассивном движении конечностью отмечаются своеобразное мышечное сопротивление вследствие повышения тонуса мышц-антагонистов, феномен «зубчатого колеса» (возникает впечатление, что суставная поверхность состоит из сцепления двух зубчатых колес). Повышение тонуса мыщц-антагонистов при пассивных движениях можно определить следующим приемом: если поднять голову лежащего, а потом резко отпустить руку, то голова не упадет на подушку, а опустится относительно плавно. Иногда голова в положении лежа несколько приподнята – феномен «воображаемой подушки».
Тремор – характерный, хотя и не обязательный для синдрома паркинсонизма симптом. Это ритмичное, регулярное, непроизвольное дрожание конечностей, лицевой мускулатуры, головы, нижней челюсти, языка, более выраженное в покое, уменьшающееся при активных движениях. Частота колебаний 4—8 в секунду. Иногда отмечаются движения пальцами в виде «скатывания пилюль», «счета монет». Тремор усиливается при волнениях, практически исчезает во сне.
Психические нарушения проявляются утратой инициативы, активности, сужением кругозора и интересов, резким понижением различных эмоциональных реакций и аффектов, а также некоторой поверхностью и медлительностью мышления (брадифрения). Наблюдаются брадипсихия – трудное активное переключение с одной мысли на другую, акайрия – прилипчивость, вязкость, эгоцентризм. Иногда возникают пароксизмы психического возбуждения.
Вегетативные нарушения проявляются в виде сальности кожи лица и волосистой части головы, себореи, гиперсаливации, гипергидроза, трофических нарушений в дистальных отделах конечностей. Выявляется нарушение постуральных рефлексов. Иногда специальными методами исследования определяется нерегулярное по частоте и глубине дыхание. Сухожильные рефлексы, как правило, без отклонений. При атеросклеротическом и постэнцефалитическом паркинсонизме могут определяться повышение сухожильных рефлексов и другие признаки пирамидной недостаточности. При постэнцефалитическом паркинсонизме встречаются так называемые окулогирные кризы – фиксация взора кверху в течение нескольких минут или часов; иногда голова при этом запрокинута. Кризы могут сочетаться с нарушением конвергенции и аккомодации (прогрессирующий супрануклеарный паралич).
Принято различать несколько клинических форм дрожательного паралича и паркинсонизма; ригидно-брадикинетическую, дрожательно-ригидную и дрожательную. Ригидно-брадикинетическая форма характеризуется повышением тонуса мышц по пластическому типу, прогрессирующим замедлением активных движений вплоть до обездвиженности; появляются мышечные контрактуры, флексорная поза больных. Эта форма паркинсонизма, наиболее неблагоприятная по течению, чаще наблюдается при атеросклеротическом и реже при постэнцефалитическом паркинсонизме. Дрожательно-ригидная форма характеризуется тремором конечностей, преимущественно их дистальных отделов, к которому с развитием заболевания присоединяется скованность произвольных движений. Для дрожательной формы паркинсонизма характерно наличие постоянного или почти постоянного средне– и крупноамплитудного тремора конечностей, языка, головы, нижней челюсти. Тонус мышц нормальный или несколько повышен. Темп произвольных движений сохранен. Эта форма чаще встречается при постэнцефалитическом и посттравматическом паркинсонизме.
У человека нарушаются движения, мышечный контроль и баланс тела в пространстве. Формируется такое состояние как-раз из-за разрушения скопления части нервных клеток (чёрная субстанция) ствола головного мозга. Эти нервные клетки соединены своими волокнами с обоими полушариями головного мозга. В них происходит выработка и высвобождение особых веществ (нейротрансмиттеры), которые помогают контролировать движения и координацию тела в пространстве. Их отсутствие и приводит к появлению таких внешне заметных признаков паркинсонизма, как снижение объёма движений с повышением тонуса мышц, дрожание конечностей, маскообразное выражение лица, хождение мелкими шажками и подобных симптомов.
Данные лабораторных и функциональных исследований.
При посттравматическом паркинсонизме выявляется повышение давления цереброспинальной жидкости при нормальном клеточном и белковом ее составе. При паркинсонизме, возникающем вследствие отравления окисью углерода, в крови обнаруживается карбоксигемоглобин, при марганцевом паркинсонизме – следы марганца в крови, моче, цереброспинальной жидкости. Глобальная электромиография при дрожательном параличе и паркинсонизме выявляет нарушение электрогенеза мышц – повышение биоэлектрической активности мышц в покое и наличие ритмических групповых разрядов потенциалов. При электроэнцефалографии обнаруживаются преимущественно диффузные негрубые изменения биоэлектрической активности головного мозга.
Диагностика и дифференциальный диагноз паркинсонизма.
В первую очередь врач проводит осмотр пациентаи уже по этим данным может поставить предварительный диагноз. Следует дифференцировать болезнь Паркинсона от синдрома паркинсонизма. Для постэнцефалитического паркинсонизма характерны глазодвигательные симптомы; могут наблюдаться кривошея, явления торсионной дистонии, которые никогда не наблюдаются при дрожательном параличе. Встречаются нарушения сна, дыхательные дискинезии с приступами зевоты, кашля, адипозогенитальные нарушения, вегетативные пароксизмы. Посттравматический паркинсонизм достоверно можно диагностировать у больных молодого и среднего возраста. Заболевание развивается после тяжелой, иногда повторной черепно-мозговой травмы. Для посттравматического паркинсонизма нехарактерны антеретропульсии, судорога взора, расстройства жевания, глотания, дыхания, каталептоидные явления. В то же время часто встречаются вестибулярные расстройства, нарушение интеллекта и памяти, зрительные галлюцинации (вследствие поражения коры большого мозга). Нередко отмечаются регредиентное течение или стабилизация патологического процесса. Для диагностики марганцевого паркинсонизма имеют значение анамнез (сведения о работе в контакте с марганцем или его окислами), обнаружение марганца в биологических жидкостях. Диагностика оксиуглеродного паркинсонизма базируется на определении в крови карбоксигемоглобина.
При атеросклеротическом паркинсонизме дрожание и ригидность сочетаются с признаками церебрального атеросклероза или возникают после острых нарушений мозгового кровообращения. Выявляются очаговые неврологические симптомы в виде пирамидной недостаточности, выраженных псевдобульбарных симптомов. Часто определяется унилатеральность ригидности и скованности. В крови обнаруживается дислипидемия, характерная для атеросклероза. Регистрируются определенные изменения РЭГ в виде уплощения пульсовых волн.
Клиническая картина, напоминающая болезнь Паркинсона, может наблюдаться при сенильной атеросклеротической деменции, для которой наиболее характерны грубые психические расстройства вплоть до деменции. Ригидность и скованность выражены умеренно, тремор, как правило, отсутствует. Отдельные клинические проявления паркинсонизма могут обнаруживаться при других наследственно-дегенеративных заболеваниях нервной системы: атаксии Фридрейха, оливопонтоцеребеллярной атрофии, ортостатической гипокинезии, болезни Крейтцфельда-Якоба. При этих заболеваниях наряду с акинетико-ригидными симптомами имеются прогрессирующие явления мозжечковой атаксии.
При недостаточности неврологического осмотра для уточнения диагноза могут быть использованы методы:
- РЭГ, УЗДГ сосудов шеи и головного мозга
- рентгенография шейного отдела позвоночника с функциональными пробами
- МРТ головного мозга и его сосудов
- МРТ шейного отдела позвоночника и т.д.
начинается Паркинсонизм в 45-52 года, когда значительно снижается активность допаминергических структур. Это болезнь нейромедиаторного обмена – недостаточно вырабатывается дофамин в базальных ганглиях и при потере 70% дофамина в стриатуме (хвостатом ядре и скорлупе) появляются клинические признаки паркинсонизма. Единственный надежный критерий диагностики – это позитронно – эмиссионная томография. На практике используется специфическая реакция на леводопу, прием которой приводит к исчезновению симптомов заболевания.
Течение и прогноз болезни Паркинсона и паркинсонизма.
Заболевание неуклонно прогрессирует. Исключение составляют некоторые формы, обусловленные лекарственными интоксикациями (при отмене препаратов может наступить улучшение состояния). Общепризнано, что лечение в начальной стадии позволяет уменьшить выраженность симптомов, замедлить прогрессирование заболевания. В поздних стадиях лечебные мероприятия менее эффективны. Заболевание приводит к инвалидизации в течение нескольких лет. Даже лечение леводопой в настоящее время замедляет течение на непродолжительное время. Это подтверждает положение, что в основе заболевания лежит не только первичный биохимический дефект, но и еще не изученный нейропатологический процесс.
Лечение болезни Паркинсона и паркинсонизма.
Лечение больных с дрожательным параличом и синдромом паркинсонизма должно быть комплексным, длительным и включать специфические антипаркинсонические препараты, седативные средства, физиотерапевтические процедуры, лечебную физкультуру, психотерапию с учетом этиологического фактора, возраста больных, клинической формы и стадии болезни, а также наличия сопутствующих заболеваний. При легких формах вначале назначают амантадин (мидантан) и парасимпатолитики, так как они вызывают меньше побочных явлений. Применяют центральные парасимпатолитики (циклодол, наркопан), пиридоксин, амантадин, агонисты дофаминовых рецепторов (бромокриптин, лизурид).
При выраженных клинических проявлениях паркинсонизма в настоящее время базисным препаратом является леводопа, обычно в сочетании с ингибитором декарбоксилазы. Дозы увеличивают медленно, в течение нескольких недель, до получения клинического эффекта. Побочные действия препарата – дистонические нарушения и психозы. Леводопа, попадая в ЦНС, декарбоксилируется в допамин, необходимый для нормальной функции базальных ганглиев. Препарат влияет прежде всего на акинезию и в меньшей степени – на другие симптомы. При сочетании леводопы с ингибитором декарбоксилазы можно уменьшить дозу леводопы и тем самым уменьшить риск развития побочных явлений.
В арсенале симптоматических антипаркинсонических средств большое место занимают холинолитические препараты, которые, блокируя м– и н-холинорецепторы, способствуют расслаблению поперечнополосатой и гладкой мускулатуры, уменьшают насильственные движения и явления брадикинезии. Это естественные и синтетические атропиноподобные препараты: беллазон (ромпаркин), норакин, комбипарк. Применяют также препараты фенотиазинового ряда: динезин, депаркол, парсидол, дипразин. Основная причина многообразия медикаментозных препаратов, используемых для лечения паркинсонизма, в недостаточной их лечебной эффективности, наличии побочных явлений, индивидуальной непереносимости и быстром привыкании к ним.
Морфологические и биохимические изменения при болезни Паркинсона настолько сложны, а течение заболевания и его последствия настолько тяжелы, а еще и усугубляются эффектами заместительной терапии - леводопой, что лечение таких больных считается верхом врачебного мастерства и подвластно виртуозам – неврологам. Поэтому открыты и работают специальные центры по лечению паркинсонизма, где уточняется диагноз, ведется наблюдение, подбираются дозы необходимых препаратов и схемы лечения. Самостоятельно назначать и принимать препараты нельзя.
Для заместительной терапии используют леводопу, карбидопу, наком. Стимулирует выброс дофамина адамантин, мемантин, бромкриптин, тормозят процесс обратного захвата допамина – антихолинэстеразные препараты и трициклические антидепрессанты (амитриптиллин), тормозит процесс распада дофамина селегилин, нейропротекторами ДА- нейронов используются антиоксиданты – селегилин, токоферол, блокаторы кальциевых каналов – нифидипин. На ранних стадиях для сохранения качества жизни доказано применение прамипексола (мирапекса). Он является препаратом первой линии лечения болезни паркинсона с высоким уровнем эффективности и безопасности. В лечении используется юмекс, неомидантан, нейропротекторы, антиоксиданты. Больным необходима лечебная гимнастика по индивидуальной программе – как можно больше двигаться и дольше сохраняться активными.
Хирургическое лечение болезни Паркинсона и паркинсонизма.
Несмотря на большие успехи, достигнутые в медикаментозном лечении паркинсонизма, возможности его в ряде случаев ограничены.
Наиболее широко применяемый препарат леводопа в большей степени способствует устранению таких симптомов болезни, как акинезия, общая скованность, в меньшей степени он влияет на ригидность мышц и тремор. Приблизительно у 25 % больных этот препарат практически неэффективен или плохо переносится.
В этих случаях возникают показания для стереотаксической операции на подкорковых узлах. Обычно производится локальное разрушение вентролатерального ядра зрительного бугра, субталамических структур или бледного шара.
С помощью операции удается в большинстве случаев добиться положительного эффекта – снижения мышечного тонуса, ослабления или прекращения тремора, уменьшения гипокинезии.
Операция обычно выполняется на стороне, противоположной той, на которой преобладают симптомы паркинсонизма. При показаниях производится двустороннее разрушение подкорковых структур.
В последние годы для лечения паркинсонизма используется также имплантация эмбриональной ткани надпочечника в полосатое тело. О клинической эффективности таких операций пока говорить преждевременно.
Стереотаксические операции на подкорковых структурах применяются также и при других заболеваниях, сопровождающихся насильственными движениями (гемибаллизм, хореоатетоз, кривошея и некоторые другие).
Трудоспособность при паркинсонизме зависит от степени выраженности двигательных нарушений, вида профессиональной деятельности. При легких и умеренных нарушениях двигательных функций больные длительно сохраняют трудоспособность при различных видах умственного труда, а также работах, не связанных с физическим напряжением и выполнением точных и координированных движений. При выраженных проявлениях заболевания больные нетрудоспособны и нуждаются в посторонней помощи.
Лечебная физкультура
У больных могут развиваться суставные контрактуры в результате нарушения тонуса и гипокинезии, например, плече – лопаточный периартроз. Больным рекомендуется низкохолестериновая диета и низкобелковая диета. Для нормального всасывания леводопы белковые продукты нужно принимать не раньше, чем через час после приема лекарства. Показана психотерапия, рефлексотерапия. Сохранение двигательной активности стимулирует выработку внутренних (эндогенных) нейротрансмиттеров. Ведутся научные изыскания по лечению паркинсонизма: это и стволовые и дофаминпродуцирующие клетки, и вакцина против болезни Паркинсона, хирургическое лечение – таламотомия, паллидотомия, высокочастотная глубинная стимуляция субталамическго ядра или внутреннего сегмента бледного шара и новые фармакологические препраты.
Физиотерапия при болезни Паркинсона и паркинсонизма
Помимо консервативного ихирургического лечения болезни Паркинсона и паркинсонизма широко практикуется физиотерапия, мануальная терапия и рефлексотерапия, позволяюще частично или полностью устранить симптом регидности мышц шеи и рук и восстановить мышечный тонус. Также пациентам с болезнью Паркинсона рекомендована лечебная физкультура (ЛФК), занятия для эффективности лечения необходимо проводить систематически.
Профилактика болезни Паркинсона
*Ягоды могут снизить риск развития болезни Паркинсона
Новое исследование показывает, что мужчины и женщины, которые регулярно употребляют в пищу ягоды, могут иметь меньший риск развития болезни Паркинсона, в то же время мужчины также могут еще больше снизить риск, регулярно употребляя в пищу яблоки, апельсины и другие продукты, богатые питательными веществами, называемые флавоноидами.
Это исследование будет представлено на 63-й встрече Американской академии неврологии (American Academy of Neurology) в Гонолулу с 9 апреля по 16 апреля 2011 года.
Флавоноиды содержатся в растениях и фруктах и также известны под общим названием витамин Р и цитрин. Они также содержатся в ягодах, шоколаде, и в цитрусовых фруктах, например грейпфруте.
В исследовании приняли участие 49 281 мужчин и 80 336 женщин. Исследователи раздали участникам анкеты и использовали базу данных для расчета количества потребления флавоноидов. Затем они проанализировали взаимосвязь между потреблением флавоноидов и риском развития болезни Паркинсона. Они также проанализировали потребление пяти основных продуктов питания, богатых флавоноидами: чай, ягоды, яблоки, красное вино и апельсины или апельсиновый сок. За участниками наблюдали в течение от 20 до 22 лет.
В течение этого времени у 805 человек развилась болезнь Паркинсона. Среди мужчин, верхние 20 процентов, которые потребляли флавоноиды больше всех, имели примерно на 40 процентов меньше шансов развития болезни Паркинсона, чем нижние 20 процентов участников мужского пола, которые потребляли наименьшее количество флавоноидов. У женщин, не было никакой связи между общим количеством потребленных флавоноидов и развитием болезни Паркинсона. Однако когда были рассмотрены подклассы флавоноидов, было обнаружено, что регулярное потребление антоцианов, которые содержатся в основном в ягодах, связано с меньшим риском развития болезни Паркинсона у мужчин и женщин.
Консультация врача по болезни Паркинсона
Вопрос: когда нужно начать лечение болезни Паркинсона?
Ответ: подход индивидуальный. Главная цель – восстановление и как можно длительное сохранение социальной, бытовой, психологической, профессиональной адаптации больного. На ранних стадиях этого можно добиться.
Вопрос: какие наиболее ранние признаки болезни Паркинсона?
Ответ: заболевание начинается лет за 7 – 10 до появления двигательных нарушений. К не двигательным ранним проявлениям относятся снижение обоняния (ощущения запахов), депрессия, тревога, запоры, нарушения сна, боли, чаще в плечевых суставах, дискомфорт в ногах, апатия (снижение интереса к жизни и всему происходящему вокруг), повышенная утомляемость, не связанная с нагрузками.
Вопрос: циклодол применяют для лечения болезни Паркинсона?
Ответ: используется все реже из-за своих побочных эффектов, но иногда, например, при сильном слюнотечении используют.
Врач невролог Кобзева С.В.





Комментарии
Ведь перенесённая нейроинфекция (энцефалит может перейти во многие заболевания в том числе и вышеперечисленн ая). Хроническая гипоксия(хронич еские заболевания лор органов и лёгких) - фактор риска состояний провоцирующих или усугубляющих паркинсонизм.
Ревматические заболевания(скл еродермия - также характеризуется маскообразность ю лица, поражением опорно-двигател ьного аппарата гемиатрофией лица) и нарушений движений в связи с этим. Гипоксия в тяжёлых случаях может приводить к адинамии и к гиподинамии.
Возможен ли такой путь: инфекции лор органов(синусит ) -> пневмония -> проникновение в мозг-> нейроинфекция(k lebsiella, Candida, S aureus) -> тяжёлая гипоксия-> паркинсонизм, склеродермия (при отсутствии адекватного своевременно начатого лечения) ->ритуальность поведения(одни и те же время и одни и те же вопросы без интереса к содержанию, бессонница, частичная психопатизация, обездвиженность , травматизм в бытовых вопросах, нарушение быстроты реакций И общей реактивности нарушения торможения
нарушения точности движений и тремор во время точно-направлен ных движений(Пролив ать из чайника воду, зависимость мышечного тонуса (болтаются мышцы как кусок мяса в маршутке) от внешних физ факторов: иннерции, вибрации гравитации при отсутствии верного этиотропного лечения инфекции которая стала стартом запуска?
При системных ревматических заболеваниях(та кже после перенесённой инфекции и гипоксии - могут ли быть аналогичные состояния?